بيمار ١
یک پسر 14 ماهه که با کاهش سطح هوشیاری ، سیانوز محدوده لب ها و حرکات مشابه تشنج به بیمارستان مراجعه کرده است
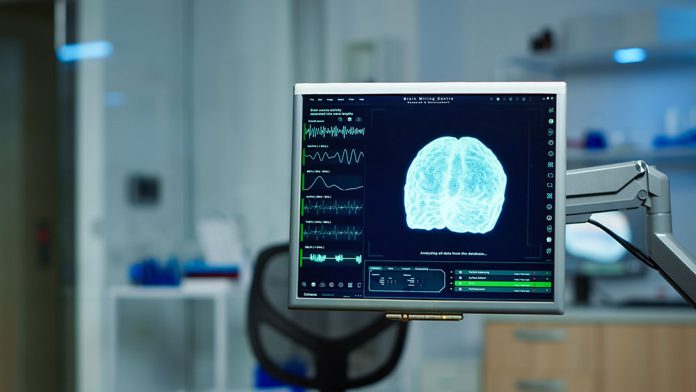
brain CT scan اولیه در بدو ورود به بیمارستان از بیمار گرفته شد که نمای :
venous hyperdense cortical vein over right parietal convexity مشهود بوده است
با اعزام به بیمارستان مجهز تر MRI/MRV برای بیمار انجام شد نتایج تصویر برداری به شرح ذیل است :
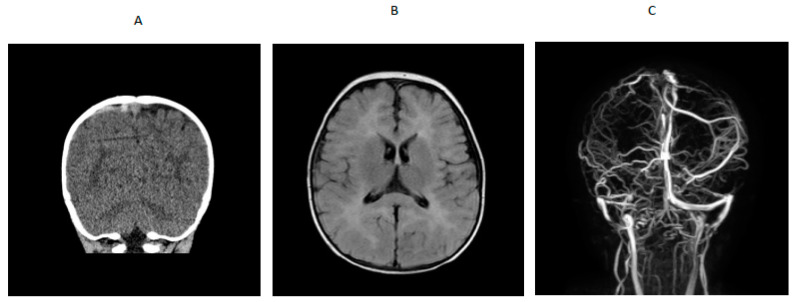
در EEG اخذ شده : generalized slowing with no epileptiform activity گزارش شد
در ابتدا برای بیمار levetiracetam تجویز و شروع شد و به علت اختلالات انعقادی ، تست های آزمایشگاهی برای وی انجام شد
بیمار با سن حاملگی 31-32 هفته بدنیا آمده ، مادر هنگام بارداری 21 سال داشته و gravida 2 و para 1 بوده است و به علت پره اکلامپسی بارداری بیمار حاصل سزارین می باشد
وزن هنگام تولد : 1820 گرم
قد : 42 سانتی متر
تست غربالگری 3 روز بعد از تولد نرمال بوده و Blood spot methionine = 26.93 µmol/L بوده است (محدوده مرجع abnormal >60 )
بیمار 24 روز در NICU مانده و سپس مرخص شده است و پس از آن هیچ گونه پیگیری دیگری نداشته است رشد و تکامل طبیعی داشته و از نظر تکاملی متناسب با سنش بوده است در حال حاضر در 14 ماهگی غلت میزند و در گفتار توانایی بیان چند کلمه را دارد وزن در صدک 84، قد در صدک 69 و دور سر در صدک 95 بود. او هیچ ویژگی فیزیکی غیرعادی نداشت.
در معاینه نورولوژیک نرمال بود هر چند که مقداری در توانایی صحبت کردن تاخیر داشت که به همین علت گفتار درمانی دریافت میکرد در طول درمان سطح هموسیستئین در محدوده 58 µmol/L تا 249 µmol/L ثبت شده است
بیمار 2
پسری 7 ساله با سابقه فشار خون بالاو رشد بالاتر از حد معمول و متناسب با سن که به علت استفراغ مداوم ، لکوسیتوز 14700 و مایکوپلاسما پنومونی بستری شده است در طی 3 روز از بستری بودن در بیمارستان تشنج های generalized tonic clonic و همی پارزی سمت چپ داشته است تصویربرداری از مغز نمای ذیل را نشان میدهد :
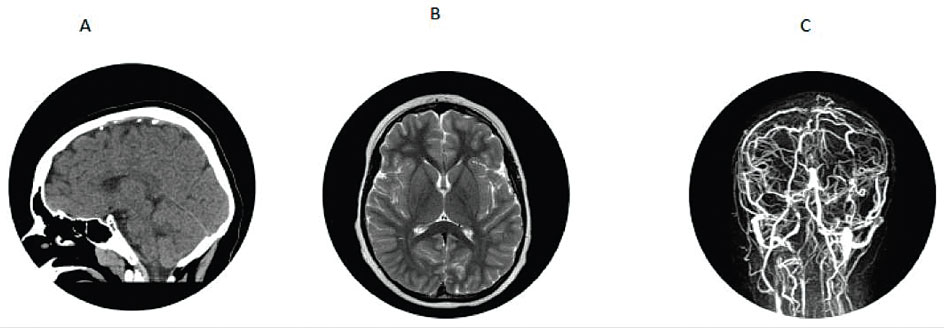
بیمار با سن حاملگی 37 هفتگی بدنیا آمده ،
وزن هنگام تولد : 3830 گرم
و 3 روز در NICU به علت تاکی پنه گذرا مانده و سپس مرخص شده است
تست غربالگری 2 روز بعد از تولد نرمال بوده و Blood spot methionine = 89.4 µmol/L بوده است (محدوده مرجع abnormal >60 )
روند تکامل :
از 15 تا 17 ماهگی شروع به را رفتن کرده است
| متغییر | بیمار 1 | بیمار2 | محدوده مرجع |
| Total homocysteine | 260.61μmol/L | 71.9 | 14.8-6.6 |
| methionine | 118µmol/L | 448µmol/L | 50-14 |
| homocysteine | 45µmol/L | 7 | 2-0 |
| Urine organic acids
/plasma acylcarnitine profile/lysosomal enzyme panel/plasma very long chain fatty acids /serum methylmalonic acid/ceroid neuronal lipofuscinosis enzymes/TPP1/PPT1\antiphospholipid antibody/antithrombin levels/protein S/prothrombin gene mutation/Factor V Leiden/β-2 glycoprotein/anti-cardiolipin antibody |
normal | normal | |
| Protein C activity | 67% | 63% | %160-80 |
| Folic acid | low | ||
| Vitamin B12 | pg/mL285 | 244 | 946-211 |
| Serum carnitines | low | ||
| RBC folate | 29.2% | 30-42% | |
| Lipoprotein lipase | 17mg/dL | <29 | |
| Serum methylmalonic acid | 0.12 | 0.15 | 0.0-0.4 µmol/L |
| glucose/serum electrolytes | normal | ||
| Ammonia | 58µmol/L | <9 | |
| lipase | 1273U/L | 23-300U/L | |
| Antithrombin lll activity | 80% | 83-128% | |
| Met/Phe ratio | 0.50 | 2 | <1 |
| Serum folate | 14.4 | 7-34.1ng/mL |
ما 2 بیمار را معرفی کردیم که 2 تا 3 روز پس از تولد،
NBS را فراموش کردهاند و در سنین بالاتر با ترومبوز ورید مغزی مراجعه کردهاند و در آنها بررسیهای متابولیک کمبود سیستاتیونین بتا-سنتاز واضح است. بیمار 1 متیونین طبیعی داشت ، نارس به دنیا آمده بود و وزن هنگام تولدش کمتر از 2000 گرم بود. بیمار 2 یک غربالگری غیرطبیعی اولیه نوزاد داشت اما آزمایش هموسیستئین تام سطح دوم روی لکه خون خشک نرمال بود، بنابراین در نظر گرفته شد که او غربالگری طبیعی برای هموسیستینوری دارد.
بیمار 1 پس از تایید تشخیص هموسیستینوری، تحت رژیم غذایی کم متیونین، اسید فولیک، ویتامین B12، ویتامین B6، مکمل بتائین و انوکساپارین قرار گرفت. MRI سریال مغز، ترومبوز ورید مغزی را با بهبود تغییرات ماده سفید در مغز نشان داد، بنابراین مصرف انوکساپارین قطع شد و روزانه 81 میلیگرم آسپرین به او داده شد. بیمار در تمام مدت بستری شدن در بیمارستان هوشیار و پایدار بود و هیچ نشانه عصبی از هیچ گونه پاتولوژی داخل جمجمه ای را پس از علائم شبه تشنج اولیه نشان نداد.
بیمار 2 برای تاخیرهای حرکتی ظریف نیاز به توانبخشی داشت. از نظر شناختی مناسب سن اش بوده است و در مدرسه عملکرد خوبی داشته است . در معاینه فیزیکی پسری قدبلند با وزن و قد بالای صدک 99 را نشان داد BMI او بالاتر از صدک 99 بود. او ویژگی های مارفانوئید را نداشت و 8 ماه پس از تشخیص HCU با کمردرد که با خم شدن به جلو و راه رفتن بدتر بود، به پزشک مراقبت های اولیه مراجعه کرد. او توسط یک جراح ستون فقرات ویزیت شد و MRI ستون فقرات شکستگی های فشاری مزمن متعدد از مهره های T6 تا L4 همراه با پوکی استخوان را نشان داد. اسکولیوز گزارش نشده است، همچنین تراکم استخوان نشان داد که معدنی شدن 82 درصد از میانگین سن و جنس است که با استئوپنی همخوانی دارد. مینرالیزاسیون هیپ چپ 96% بود که طبیعی است اما استئوپنی سر استخوان ران وجود داشت. او همچنین دچار آسیب برداشتن مچ پای راست در مقابل شکستگی قدیمی و شکستگی دیستال نازک نی چپ شده است. وی به متخصص غدد اطفال ارجاع داده شد که پس از مشورت با متخصص ژنتیک برای وی درمان pamidronate تجویز کردند. درمان HCU با غذاها و داروها همچنان در سن او چالش برانگیز است.
Homocystinuria due to cystathionine beta synthase deficiency
هموسیستینوری ها گروه ناهمگنی از اختلالات متابولیک به دلیل نقص در چرخه متابولیک متیونین هستند . اولین موردی که کشف شد و تا حد زیادی مشهورترین و شناخته شده ترین آنها است هموسیستینوری کلاسیک (HCU) است، نقص اساسی در این بیماری کاهش قابل توجه در فعالیت آنزیم کلیدی سیستاتیونین بتا سنتاز (CBS) است و از نظر بیوشیمیایی با افزایش متیونین و هموسیستئین کل و همچنین کاهش سیستاتیونین مشخص می شود.
هموسیستینوری کلاسیک ناشی از کمبود سیستاتیونین بتا سنتاز (CBS) تخمین زده می شود که 1 نوزاد از هر 200000 نوزاد در ایالات متحده را تحت تاثیر قرار میدهد، اما شیوع واقعی ممکن است بسیار بالاتر از پروتکل های غربالگری فعلی نوزادان باشد که از متیونین و در بسیاری از برنامه های غربالگری، از هموسیستئین تام استفاده می کنند. بیمارانی که در غربالگري تشخیص داده نشده اند در معرض افزایش خطر ناتوانی ذهنی، نزدیک بینی پیشرونده و به دنبال آن از دست دادن بینایی ناشی از ازدست رفتن عدسی، تغییرات اسکلتی همراه با اسکولیوز، استئوپنی و پوکی استخوان، شکستگی ها و همچنین ترومبوآمبولی همراه با سکته مغزی و ترومبوز وریدی هستند. بیمارانی که از طریق برنامههای غربالگری نوزادان شناسایی میشوند با ترکیبی از رژیم غذایی بسیار کم متیونین شامل فرمولهای پزشکی و رژیم غذایی کم پروتئین و همچنین بتائین، ویتامین B12، ویتامین B6 و فولات درمان میشوند. تخمین زده می شود که حدود 50 درصد از بیماران CBS به مکمل های ویتامین B6 پاسخ می دهند.
بسیاری از اختلالات متابولیک قابل درمان قبل از اینکه نوزادان و کودکان مبتلا علامت دار شوند، شناسایی می شوند. غربالگری معمولاً در 48 ساعت پس از زندگی در اکثر ایالت های ایالات متحده انجام می شود و برخی از ایالت ها غربالگری دوم را به عنوان یک سیاست روی همه نوزادان آزمایش شده یا بر اساس زمان انجام غربالگری اولیه انجام میدهند ، به امید اینکه شناسایی نوزادانی که ممکن است در اولین غربالگری پيدا نشده باشند میسر شود. و آنچه اهمیت دارد این است که بررسی این بیماری در افرادی که با علائم نورولوژیک مراجعه می کنند ضرورت دارد.