25-هیدروکسی ویتامین D [25(OH)D] رایج ترین شکل گردش خون ویتامین D است و غلظت سرمی آن نشان دهنده وضعیت ویتامین D است. در بسیاری از مطالعات، غلظت کم 25(OH)D به عنوان یک عامل خطر بالقوه برای چندین بیماری مزمن ریوی و همراه با کاهش عملکرد ریه، کاهش پاسخ گلوکوکورتیکوئیدی، تشدید مکرر آسم و در نتیجه افزایش استفاده از استروئیدها شناسایی شده است .
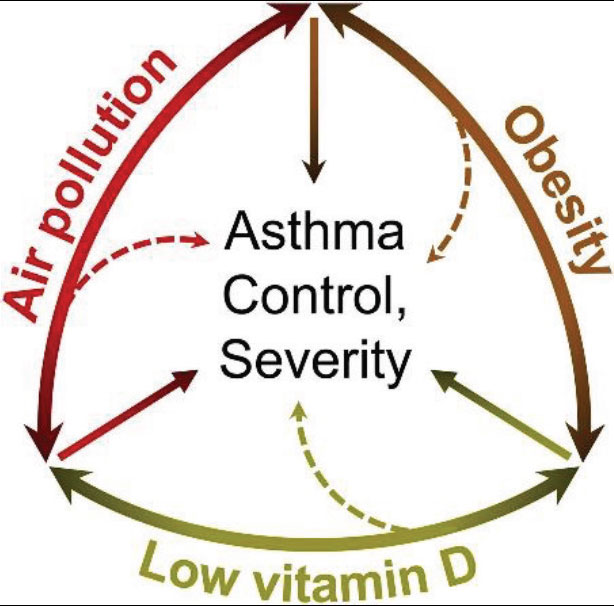
در دهه 1960، شیوع آسم و بیماری های آلرژیک در سراسر جهان شروع به افزایش کرد. در حال حاضر، بار این بیماری بیش از 300 میلیون نفر را درگیر کرده است. ما فرض می کنیم که با رشد جمعیت بیشتر، زمان بیشتری در داخل خانه سپری می شود و کمتر در معرض نور خورشید قرار می گیریم که منجر به کاهش تولید ویتامین D پوستی می شود. همراه با دریافت ناکافی از غذاها و مکمل ها، این امر منجر به کمبود ویتامین D، به ویژه در زنان باردار می شود که منجر به آسم و آلرژی بیشتر در فرزندان آنها می شود. ویتامین D با سیستم ایمنی و رشد ریه در رحم مرتبط است، و مطالعات اپیدمیولوژیک ما نشان می دهد که مصرف بیشتر ویتامین D توسط مادران باردار خطر آسم را تا 40 درصد در کودکان 3 تا 5 ساله کاهش می دهد. کمبود ویتامین D با چاقی، نژاد آفریقایی آمریکایی (به ویژه در محیط های شهری، درون شهری) و مهاجران اخیر به کشورهای غربی مرتبط است، بنابراین منعکس کننده الگوهای اپیدمیولوژیک مشاهده شده در اپیدمی آسم است. دریافت مکمل ویتامین D کافی در بارداری ممکن است به کاهش قابل توجهی در بروز آسم در کودکان خردسال منجر شود.
طبق مطالعات قبلی، میانگین شیوع آسم در ایران 4/13 درصد است. آسم شدید در زنان دو تا سه برابر بیشتر از مردان است. آسم دوران کودکی در پسران شایع تر است اما در دوران نوجوانی در دختران شایع تر است و این الگو در بزرگسالی نیز ادامه می یابد.
آسم در جمعیت کودکان نقش مهمی در بروز عوارض و افزایش هزینه های مراقبت های بهداشتی دارد. کمبود ویتامین D3 با ایجاد آسم مرتبط است. مطالعات اخیر در مدل های بیماری های مجاری هوایی بزرگسالان نشان می دهد که متابولیت زیست فعال ویتامین D3، کلسیتریول (1،25-دی هیدروکسی ویتامین D3)، پاسخ به التهاب را تعدیل می کند.
علاقه فزاینده ای به کاربرد درمانی ویتامین D در آسم وجود دارد که با شواهد قابل توجهی در مورد ارتباط اپیدمیولوژیک بین کمبود ویتامین D و کنترل آسم پشتیبانی می شود. ویتامین D مسیرهای ایمنی متنوعی را در اندوتیپهای ناهمگن آسم تعدیل میکند، و اعمال لنفوسیتها، ماست سلها، سلولهای ارائهدهنده آنتیژن و سلولهای ساختاری را تنظیم میکند تا پاسخهای التهابی بیش از حد را کاهش دهد. آسم آلرژیک با شکست در تحمل ایمنی و ایجاد پاسخ های پاتولوژیک به آلرژن های هوای استنشاقی مشخص می شود و ویتامین D به طور گسترده نشان داده شده است که از تنظیم ایمنی حمایت می کند. سایتوکین های آلارمین به طور فزاینده ای در التهاب ائوزینوفیلیک غیر آلرژیک که ویتامین D آن را نیز تنظیم می کند، دخیل هستند. مقاومت استروئیدی و پاسخ های پاتولوژیک اینترلوکین (IL)-17 از ویژگی های آسم شدید هستند و ویتامین D به طور مفیدی پاسخ به استروئیدها را در این افراد افزایش می دهد. علاوه بر این، ویتامین D مسیرهای ضد میکروبی را تقویت می کند، که با تشدید آسم ناشی از عفونت مرتبط است. این مکانیسم ها از نقش ویتامین D به عنوان پیشگیری ثانویه برای کاهش تشدید و التهاب در آسم حمایت می کنند. مکانیسمهای مشابه و اثرات روی رشد ریه جنین، احتمالاً زمینه ساز نقش درمانی پیشگیری اولیه در بارداری برای ویتامین D برای کاهش رشد آسم در کودکان است. نکته مهم این است که در بررسی سیستماتیک آزمایشها تا به امروز، ویتامین D برای آسم مفید است. شواهد مورد بحث در این بررسی از اهمیت بهینه سازی ویتامین D در مراقبت جامع آسم حمایت می کند.
در ادامه به مروری بر دو مقاله با موضوع اثربخشی ویتامین D در روند درمان بیماری آسم می پردازیم.
در این مقاله ردنی دی و همکاران از سلولهای ماهیچه صاف راه هوایی جنین انسان (ASM) به عنوان مدلی از راه هوایی پس از تولد اولیه استفاده کردند تا چگونگی تعدیل کلسیتریول در بازسازی ایجاد شده توسط سایتوکینهای پیش التهابی را بررسی کنند. سلول ها از قبل با کلسیتریول تیمار شدند و سپس تا 72 ساعت در معرض TNFα یا TGFβ قرار گرفتند. فعالیت متالوپروتئیناز ماتریکس (MMP)، تولید ماتریکس خارج سلولی (ECM)، و تکثیر سلولی مورد بررسی قرار گرفت. کلسیتریول افزایش بیان TNFαF و فعالیت MMP-9 را کاهش داد. علاوه بر این، کلسیتریول بیان و رسوب کلاژن III ناشی از TNFα و TGFβ را کاهش داد و به طور جداگانه، تکثیر سلولهای ASM جنینی ناشی از هر یک از واسطههای التهابی را مهار کرد.
تجزیه و تحلیل مسیرهای سیگنالینگ نشان داد که اثرات کلسیتریول در ASM جنینی شامل سیگنال دهی ERK است، اما نه سایر مسیرهای التهابی اصلی. به طور کلی، داده ها نشان میدهد که کلسیتریول میتواند اثرات متعدد TNFα و TGFβ را در توسعه راه هوایی کاهش دهد و به یک رویکرد بالقوه جدید برای کاهش تغییرات ساختاری در بیماریهای التهابی راه هوایی دوران کودکی اشاره میکند.
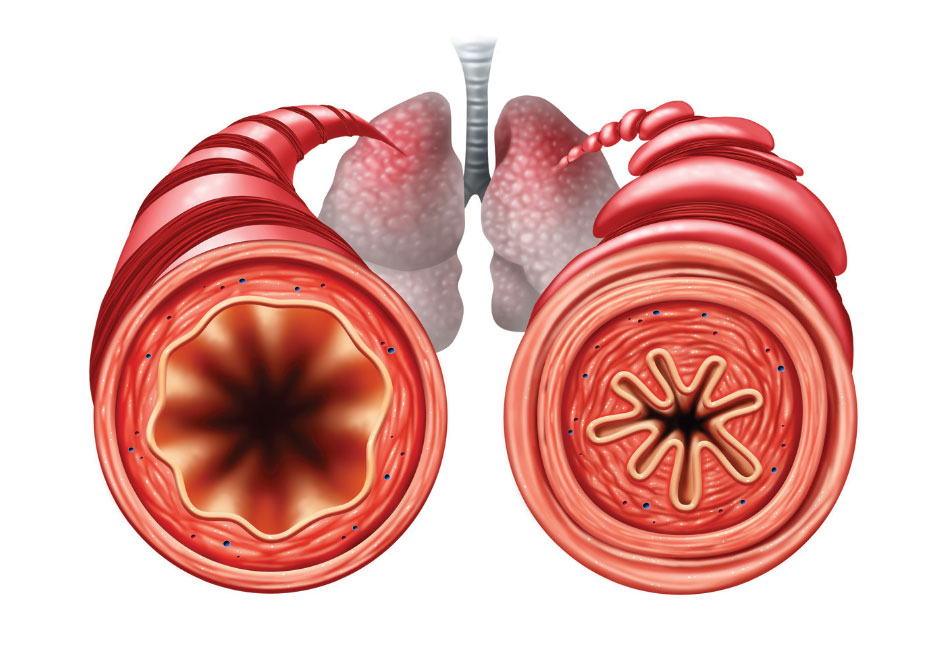
در مطالعه ای دیگر، دکتر صبا ارشی و همکاران بررسی بر روی 130 فرد، 10 تا 50 ساله ساکن تهران در یک دوره 24 هفته ای انجام دادند. اطلاعات مربوط به سن، جنس، نمایه توده بدنی، مرحله آسم، IgE کل سرم، سابقه رینیت آلرژیک، درماتیت آتوپیک، آلرژی غذایی و کهیر جمع آوری شد.
پارامترهای اسپیرومتری (حجم بازدم اجباری در 1 ثانیه [FEV1] و نسبت FEV1 به ظرفیت حیاتی اجباری) و اندازهگیری ویتامین D سرم قبل و 8 و 24 هفته بعد از مداخله بهدست آمد. بیماران به طور تصادفی به 2 گروه تقسیم شدند. هر دو گروه با توجه به مرحله مربوطه کنترل کننده های آسم (بودزوناید یا بودزونید به اضافه فرموترول) را دریافت کردند، اما گروه مداخلهT مکمل ویتامین D (100000 واحد بولوس عضلانی به اضافه 50000 واحد در هفته به صورت خوراکی) را علاوه بر کنترل کننده های آسم دریافت کردند.
FEV1 به طور قابل توجهی در هر دو گروه پس از 8 هفته بهبود یافت، اما تفاوت معنی داری بین 2 گروه در ابتدا (20/0 = P) یا بعد از 8 هفته (99/0 = P) مشاهده نشد. با این حال، بهبود قابل توجهی در گروه مداخله در 16 هفته گذشته مشاهده شد و FEV1 در گروه مداخله به طور قابل توجهی پس از 24 هفته بهتر از گروه دیگر بود (001/0 > P).
نتیجه
استفاده از مکمل ویتامین D همراه با دارو درمانی آسم می تواند به طور قابل توجهی FEV1 را در آسم پایدار، خفیف تا متوسط پس از 24 هفته بهبود بخشد.
Comparison of clinical factors in patients with asthma in two groups and in patients with vitamin D insufficiency and patients with vitamin D deficiency
| Variables | Case | Control | P1 | P2 | P3 | ||||
| Total (n=66) | Insufficient (n=33) | Deficient (n=33) | Total (n=66) | Insufficient (n=33) | Deficient (n=33) | ||||
| ACT score | |||||||||
| Before | 11.26±3.66 | 11.73±3.56 | 10.79±0.65 | 11.69±3.75 | 11.58±3.62 | 11.81±3.94 | 0.307 | 0.923 | 0.504 |
| 3 months later | 13.30±4.51 | 13.18±4.65 | 13.42±4.44 | 11.45±3.63 | 11.61±3.74 | 11.78±3.57 | 0.812 | 0.752 | 0.011 |
| P4 | <0.001 | 0.014 | 0.002 | 0.486 | 0.956 | 0.236 | |||
| 25(OH)D (ng/ml) | |||||||||
| Before | 17.04±6.42 | 23.42±2.64 | 11.29±0.79 | 17.17±6.59 | 23.64±3.26 | 11.36±0.75 | <0.001 | <0.001 | 0.862 |
| 3 months later | 34.88±8.04 | 36.36±11.33 | 33.54±2.68 | 17.34±6.17 | 23.43±2.96 | 11.88±0.71 | 0.184 | <0.001 | <0.001 |
| P4 | <0.001 | <0.001 | <0.001 | 0.102 | 0.167 | 0.054 | |||
| FVC (%) | |||||||||
| Before | 79.76±9.17 | 79.27±9.37 | 81.67±7.63 | 79.03±10.47 | 80.27±9.33 | 79.91±10.23 | 0.405 | 0.117 | 0.589 |
| 3 months later | 81.29±7.13 | 80.91±6.68 | 81.52±9.95 | 80.47±9.59 | 81.06±10.53 | 80.88±10.55 | 0.922 | 0.052 | 0.536 |
| P4 | 0.098 | <0.001 | 0.125 | 0.166 | 0.107 | 0.506 | |||
| FEV1 (%) | |||||||||
| Before | 71.76±7.70 | 73.52±8.01 | 70.00±7.07 | 72.12±8.04 | 71.12±7.25 | 73.12±8.76 | 0.069 | 0.300 | 0.791 |
| 3 months later | 74.17±10.16 | 72.85±15.77 | 75.48±9.98 | 72.55±8.82 | 73.09±9.60 | 72.00±8.08 | 0.343 | 0.694 | 0.041 |
| P4 | 0.130 | 0.796 | 0.003 | 0.658 | 0.172 | 0.376 | |||
| FEV 1 / FVC (%) | |||||||||
| Before | 74.89±5.99 | 75.58±5.17 | 74.21±6.73 | 73.95±6.54 | 73.97±6.93 | 73.94±6.22 | 0.381 | 0.984 | 0.391 |
| 3 months later | 80.08±11.13 | 80.15±10.54 | 80.00±11.85 | 75.37±12.09 | 77.44±10.83 | 73.36±6.43 | 0.958 | 0.160 | 0.022 |
| P4 | <0.001 | 0.006 | 0.008 | 0.447 | 0.322 | 0.531 | |||
Abbreviate: ACT score: Asthma Control Test score; FEV1: Forced Expiratory Volume in one second; FVC: Forced Vital Capacity
P1: The significant level of comparison two subgroups insufficient vitamin D with deficient in Case group
P2: The significant level of comparison two subgroups insufficient vitamin D with deficient in Control group
P3: The significant level of comparison two groups study (Case group with Control group)
P4: The significant level of comparison between before and 3 months later in each groups and subgroups


